Совет 1: Как писать ионные уравнения
С точки зрения теории электролитической диссоциации, растворы некоторых соединений способны проводить электрический ток, потому что распадаются на правильные и негативные частицы – ионы. Такие вещества именуются электролитами, к которым дозволено отнести соли, кислоты, основания. Множество химических реакций протекает в растворах, а значит, между ионами, потому надобно уметь положительно писать ионные уравнения .

Вам понадобится
- – таблица растворимости солей, кислот, оснований.
Инструкция
1. Раньше чем приступать к написанию ионных уравнений, нужно усвоить некоторые правила. Нерастворимые в воде, газообразные и малодиссоциирующие вещества (скажем, вода) на ионы не распадаются, а значит, записывайте их в молекулярном виде. Также сюда относятся слабые электролиты, такие как H2S, H2CO3, H2SO3, NH4OH. Растворимость соединений дозволено узнать по таблице растворимости, которая является разрешенным справочным материалом на всех видах контроля. Там же указаны все заряды, которые присущи катионам и анионам. Для полновесного выполнения задания нужно написать молекулярное, ионное полное и ионное сокращенное уравнения .
2. Пример № 1. Напишите реакцию нейтрализации между серной кислотой и гидроксидом калия, разглядите ее с точки зрения ТЭД (теории электролитической диссоциации). Вначале запишите уравнение реакции в молекулярном виде и расставьте показатели.H2SO4 + 2KOH = K2SO4 + 2H2OПроанализируйте полученные вещества на их растворимость и диссоциацию. Все соединения растворимы в воде, а значит диссоциируют на ионы. Исключение только вода, которая на ионы не распадается, следственно, останется в молекулярном виде.Напишите ионное полное уравнение, обнаружьте идентичные ионы в левой и правой части и подчеркните. Дабы сократить идентичные ионы, зачеркните их.2H+ +SO4 2- +2K+ +2OH- = 2K+ +SO4 2- + 2H2OВ итоге получится ионное сокращенное уравнение:2H+ +2OH- = 2H2OКоэффициенты в виде двоек также дозволено сократить:H+ +OH- = H2O
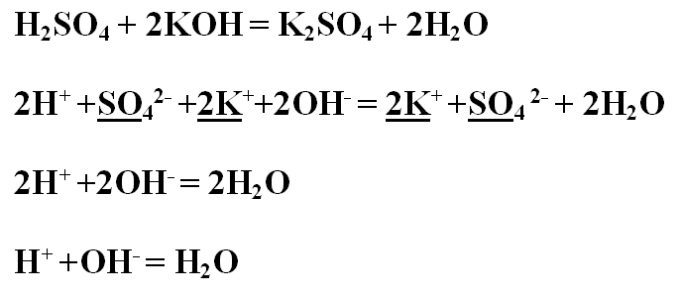
3. Пример № 2. Напишите реакцию обмена между хлоридом меди и гидроксидом натрия, разглядите ее с точки зрения ТЭД. Запишите уравнение реакции в молекулярном виде и расставьте показатели. В итоге, образовавшийся гидроксид меди вывалился в осадок голубого цвета. CuCl2 + 2NaOH = Cu(OH) 2? +2NaClПроанализируйте все вещества на их растворимость в воде – растворимы все, помимо гидроксида меди, тот, что на ионы диссоциировать не будет. Запишите ионное полное уравнение, подчеркните и сократите идентичные ионы:Cu2+ +2Cl- + 2Na+ +2OH- = Cu(OH) 2?+2Na+ +2Cl-Остается ионное сокращенное уравнение:Cu2+ +2OH- = Cu(OH) 2?
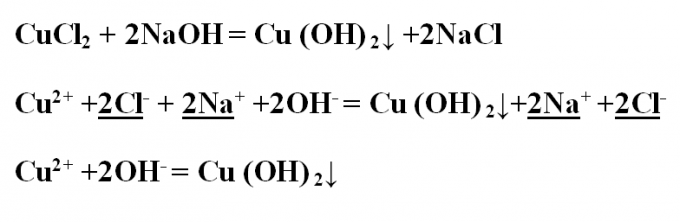
4. Пример № 3. Напишите реакцию обмена между карбонатом натрия и соляной кислотой, разглядите ее с точки зрения ТЭД. Запишите уравнение реакции в молекулярном виде и расставьте показатели. В итоге реакции образуется хлорид натрия и выдается газообразное вещество СО2 (углекислый газ либо оксид углерода (IV)). Оно образуется за счет разложения слабой угольной кислоты, распадающейся на оксид и воду. Na2CO3 + 2HCl = 2NaCl + CO2?+H2OПроанализируйте все вещества на их растворимость в воде и диссоциацию. Углекислый газ уходит из системы, как газообразное соединение, вода – это малодиссоциирующее вещество. Все остальные вещества на ионы распадаются. Запишите ионное полное уравнение, подчеркните и сократите идентичные ионы:2Na+ +СO3 2- +2H+ +2Cl- =2Na+ +2Cl- +CO2?+H2OОстается ионное сокращенное уравнение:СO3 2- +2H+ =CO2?+H2O
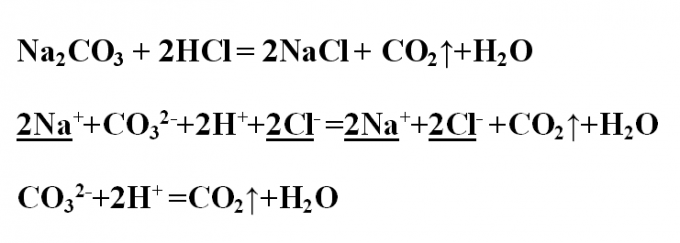
Совет 2: Как составить уравнения реакций по химии
Уравнение реакции – условная запись химического процесса, при котором одни вещества превращаются в другие с изменением свойств. Для записи химических реакций применяют формулы веществ и умения о химических свойствах соединений.

Инструкция
1. Верно напишите формулы, в соответствии с их наименованиями. Скажем, оксид алюминия Al?O?, индекс 3 от алюминия (соответствует его степени окисления в этом соединении) поставьте вблизи кислорода, а индекс 2 (степень окисления кислорода) вблизи алюминия. Если степень окисления +1 либо -1, то индекс не ставится. К примеру, вам надобно записать формулу нитрата аммония. Нитрат – кислотный остаток азотной кислоты (-NO?, с.о. -1), аммоний (-NH?, с.о. +1). Таким образом формула нитрата аммония – NH? NO?. Изредка степень окисления указывается в наименовании соединения. Оксид серы (VI) – SO?, оксид кремния (II) SiO. Некоторые примитивные вещества (газы) записываются с индексом 2: Cl?, J?, F?, O?, H? и т.д.
2. Нужно знать, какие вещества вступают в реакцию. Видимые знаки реакции: выделение газа, метаморфоза окраски и выпадение осадка. Дюже зачастую реакции проходят без видимых изменений. Пример 1: реакция нейтрализацииH?SO? + 2 NaOH ? Na?SO? + 2 H?OГидроксид натрия реагирует с серной кислотой с образованием растворимой соли сульфата натрия и воды. Ион натрия отщепляется и соединяется с кислотным остатком, замещая водород. Реакция проходит без внешних знаков. Пример 2: йодоформная проба С?H?OH + 4 J? + 6 NaOH?CHJ?? + 5 NaJ + HCOONa + 5 H?OРеакция идет в несколько этапов. Финальный итог – выпадение кристаллов йодоформа желтого цвета (добротная реакция на спирты). Пример 3: Zn + K?SO? ? Реакция немыслима, т.к. в ряду напряжений металлов цинк стоит позже калия и не может вытеснять его из соединений.
3. Закон сохранения массы гласит: масса веществ, вступивших в реакцию, равна массе образовавшихся веществ. Грамотная запись химической реакции – половина триумфа. Нужно расставить показатели. Начните уравнивать с тех соединений, в формулах которых присутствуют крупные индексы. K?Cr?O? + 14 HCl ? 2 CrCl? + 2 KCl + 3 Cl?? + 7 H?O Расставлять показатели начните с бихромата калия, т.к. в его формуле содержится крупнейший индекс (7). Такая точность в записи реакций нужна для расчета массы, объема, концентрации, выделившейся энергии и других величин. Будьте внимательны. Запомните особенно зачастую встречающиеся формулы кислот и оснований, а также кислотные остатки.
Совет 3: Как написать уравнение в ворде
Работу с формулами и уравнениями в офисном приложении Word, входящем в пакет Microsoft Office, обеспечивает особая утилита «Редактор формул», являющаяся частью программы Math Type.

Инструкция
1. Нажмите кнопку «Пуск» для вызова основного меню системы и перейдите в пункт «Все программы».
2. Укажите пункт Microsoft Office и запустите приложение Word.
3. Вызовите контекстное меню панели инструментов кликом правой кнопки мыши и укажите пункт «Настройка».
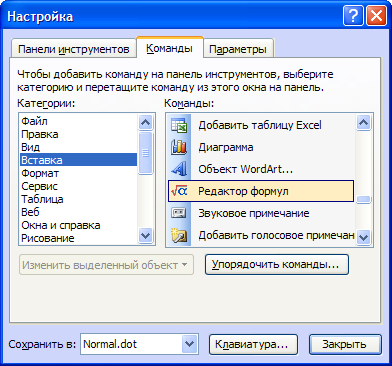
4. Перейдите на вкладку «Команды» открывшегося диалогового окна настроек и выберите пункт «Вставка» в разделе «Категории».
5. Укажите «Редактор формул» и перетащите элемент в всякое свободное место панели инструментов окна приложения Word.
6. Закройте все открытые окна программ при неосуществимости выявления утилиты «Редактор формул» и раскройте узел «Установка и удаление программ» на панели управления операционной системы двойным кликом мыши для установки требуемого инструмента.
7. Укажите приложение в списке установленных программ и нажмите кнопку «Заменить».
8. Укажите команду «Добавить либо удалить компоненты» и удостоверите свой выбор нажатием кнопки «Дальше».
9. Примените флажок на поле «Расширенная настройка приложений» и удостоверите выполнение команды нажатием кнопки «Дальше».
10. Раскройте меню «Средства Office» и укажите пункт «Редактор формул».
11. Выберите опцию «Запускать с моего компьютера» и закончите работу программы.
12. Вернитесь в основное меню «Пуск» и перейдите в пункт «Исполнить» для редактирования параметра масштабирования утилиты «Редактор формул».
13. Введите значение regedit в поле «Открыть» и исполните одновременное нажатие функциональных клавиш CTRL+А.
14. Введите значение forceopen в текстовое поле окна поиска и нажмите кнопку OK для подтверждения выполнения команды.
15. Раскройте обнаруженный элемент forceopen двойным кликом мыши и измените значение параметра на 1.
16. Закончите работу редактора реестра и вернитесь в основное окно офисного приложения Microsoft Word.
17. Нажмите добавленную кнопку редактора формул в панели инструментов и измените масштаб для комфорта вступления формул.
Видео по теме
Обратите внимание!
Дабы верно определить число ионов, надобно показатель, стоящий перед формулой, умножить на индекс.
Полезный совет
В уравнениях реакций неукоснительно проверяйте показатели.










