- Совет 1: Как определить тип кристаллической решетки
- Инструкция
- Совет 2: Как определить температуру плавления
- Инструкция
- Совет 3: Какие виды у кристаллических решеток
- Кристаллы
- Ионные кристаллические решетки
- Атомные кристаллические решетки
- Молекулярные кристаллы
- Металлические кристаллические решетки
- Совет 4: Какая кристаллическая решетка у алмаза
- Инструкция
Совет 1: Как определить тип кристаллической решетки
Кристалл – это тело, частицы которого (атомы, ионы, молекулы) располагаются не в хаотичном, а в сурово определенном порядке. Данный порядок периодично повторяется, образуя как бы воображаемую «решетку». Принято считать, что существует четыре типа кристаллических решеток: металлические, ионные, ядерные и молекулярные. А как дозволено определить, какой тип кристаллической решетки имеет то либо иное вещество?
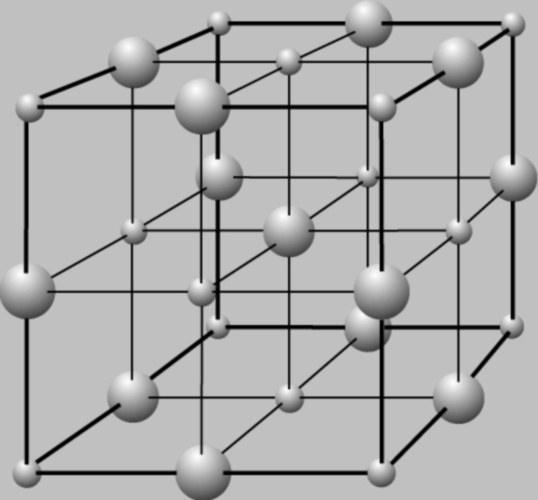
Инструкция
1. Как легко дозволено додуматься из самого называния, металлический тип решетки встречается у металлов. Эти вещества характеризуются, как водится, высокой температурой плавления, металлическим блеском, твердостью, являются отменными проводниками электрического тока. Запомните, что в узлах решеток такого типа находятся либо нейтральные атомы либо позитивно заряженные ионы. В интервалах между узлами – электроны, миграция которых и обеспечивает высокую электропроводимость сходственных веществ.
2. Ионный тип кристаллической решетки. Следует запомнить, что он присущ оксидам и солям. Классический пример – кристаллы каждом вестимой поваренной соли, хлорида натрия. В узлах таких решеток попеременно чередуются правильно и негативно заряженные ионы. Такие вещества, как водится, тугоплавки, с малой летучестью. Как легко додуматься, они имеют ионный тип химической связи.
3. Ядерный тип кристаллической решетки присущ простым веществам – неметаллам, которые при типичных условиях представляют собою твердые тела. Скажем, сере, фосфору, углероду. В узлах таких решеток находятся нейтральные атомы, связанные друг с ином ковалентной химической связью. Таким веществам свойственна тугоплавкость, нерастворимость в воде. Некоторым (скажем, углероду в виде алмаза) – экстраординарно высокая твердость.
4. Наконец, конечный тип решетки – молекулярный. Он встречается у веществ, находящихся при типичных условиях в жидком либо газообразном виде. Как вновь-таки легко дозволено осознать из наименования, в узлах таких решеток – молекулы. Они могут быть как неполярного вида (у примитивных газов типа Cl2, О2), так и полярного вида (самый знаменитый пример – вода H2O). Вещества с таким типом решетки не проводят ток, летучи, имеют низкие температуры плавления.
5. Таким образом, дабы с уверенностью определить, какой тип кристаллической решетки имеет то либо иное вещество, вам следует разобраться, к какому классу веществ оно относится и какие физико-химические свойства имеет.
Совет 2: Как определить температуру плавления
Температуру плавления твердого вещества измеряют для определения степени его чистоты. Примеси в чистом веществе традиционно понижают температуру плавления либо увеличивают промежуток, в котором плавится соединение. Способ с применением капилляра является типичным для контроля оглавления примесей.

Вам понадобится
- – испытуемое вещество;
- – стеклянный капилляр, запаянный с одного конца (диаметром 1 мм);
- – стеклянная трубка диаметром 6-8 мм и длиной не менее 50 см;
- – нагреваемый блок.
Инструкция
1. Заранее высушенное испытуемое вещество разотрите в ступке в мельчайший порошок. Опрятно возьмите капилляр и открытым концом погрузите в вещество, при этом некоторое его число должно попасть в капилляр.
2. Поставьте стеклянную трубку вертикально на твердую поверхность и несколько раз киньте через нее капилляр запаянным концом вниз. Это содействует уплотнению вещества. Для определения температуры плавления столбик вещества в капилляре должен быть около 2-5 мм.
3. Капилляр с веществом прикрепите к термометру резиновым колечком так, дабы запаянный конец капилляра находился на ярусе ртутного шара термометра, а вещество – приблизительно на его середине.
4. Разместите термометр с капилляром в нагреваемый блок и отслеживайте за изменениями испытуемого вещества при возрастании температуры. Термометр до и в процессе нагревания не должен касаться стенок блока и других мощно нагретых поверхностей, напротив он может лопнуть.
5. Как только температура на термометре приблизится к температуре плавления чистого вещества, уменьшите нагревание, дабы не пропустить момент начала плавления .
6. Подметьте температуру, при которой возникают первые капли жидкости в капилляре (предисловие плавления ), и температуру, при которой исчезают последние кристаллы вещества (конец плавления ). В этом промежутке вещество начинает спадать до полного перехода в жидкое состояние. При проведении обзора также обратите внимание на метаморфоза цвета либо разложение вещества.
7. Повторите измерения еще 1-2 раза. Итоги всего измерения представьте в виде соответствующего температурного промежутка, в течение которого вещество переходит из твердого состояния в жидкое. В заключение обзора сделайте завершение о чистоте испытуемого вещества.
Видео по теме
Совет 3: Какие виды у кристаллических решеток
В кристаллах химические частицы (молекулы, атомы и ионы) расположены в определенном порядке, в некоторых условиях они образуют верные симметричные многогранники. Выделяют четыре типа кристаллических решеток — ионные, ядерные, молекулярные и металлические.

Кристаллы
Кристаллическое состояние характеризуется наличием далекого порядка в расположении частиц, а также симметрией кристаллической решетки. Твердыми кристаллами называют трехмерные образования, у которых один и тот же элемент конструкции повторяется во всех направлениях. Верная форма кристаллов обусловлена их внутренним строением. Если в них заменить молекулы, атомы и ионы точками взамен центров тяжести этих частиц, получится трехмерное регулярное разделение – кристаллическая решетка. Повторяющиеся элементы ее конструкции называют элементарными ячейками, а точки — узлами кристаллической решетки. Выделяют несколько типов кристаллов в зависимости от частиц, которые их образуют, а также от нрава химической связи между ними.
Ионные кристаллические решетки
Ионные кристаллы образуют анионы и катионы, между которыми есть ионная связь. К данному типу кристаллов относятся соли и гидроксиды большинства металлов. Весь катион притягивается r аниону и отталкивается от других катионов, следственно в ионном кристалле немыслимо выделить одиночные молекулы. Кристалл дозволено рассматривать как одну большую молекулу, причем ее размеры не ограничены, она способна присоединять новые ионы.
Атомные кристаллические решетки
В ядерных кристаллах отдельные атомы объединены ковалентными связями. Как и ионные кристаллы, их также дозволено рассматривать как большие молекулы. При этом ядерные кристаллы дюже твердые и крепкие, нехорошо проводят электричество и тепло. Они фактически нерастворимы, для них характерна низкая реакционная способность. Вещества с ядерными кристаллическими решетками плавятся при дюже высоких температурах.
Молекулярные кристаллы
Молекулярные кристаллические решетки образуются из молекул, атомы которых объединены ковалентными связями. Из-за этого между молекулами действуют слабые молекулярные силы. Такие кристаллы отличаются малой твердостью, низкой температурой плавления и высокой текучестью. Вещества, которые они образуют, а также их расплавы и растворы нехорошо проводят электрический ток.
Металлические кристаллические решетки
В кристаллических решетках металлов атомы расположены с максимальной плотностью, их связи являются делокализованными, они распространяются на каждый кристалл. Такие кристаллы непрозрачны, отличаются металлическим блеском, легко деформируются, при этом классно проводят электричество и тепло.Данная систематизация описывает лишь предельные случаи, множество кристаллов неорганических веществ принадлежит к промежуточным типам — молекулярно-ковалентным, ковалентно-ионным и др. В качестве примера дозволено привести кристалл графита, внутри всякого слоя у него ковалентно-металлические связи, а между слоями — молекулярные.
Совет 4: Какая кристаллическая решетка у алмаза
Алмаз – это минерал, относящийся к одной из аллотропных модификаций углерода. Отличительной чертой его является высокая твердость, которая по праву приносит ему звание самого твердого вещества. Алмаз довольно редкий минерал, но совместно с этим и самый обширно общеизвестный. Исключительная его твердость находит свое использование в машиностроении и промышленности.

Инструкция
1. Алмаз имеет ядерную кристаллическую решетку. Атомы углерода, составляющие основу молекулы, располагаются в виде тетраэдра, вследствие чему алмаз имеет такую высокую крепкость. Все атомы связаны крепкими ковалентными связями, которые образуются, исходя из электронного строения молекулы.
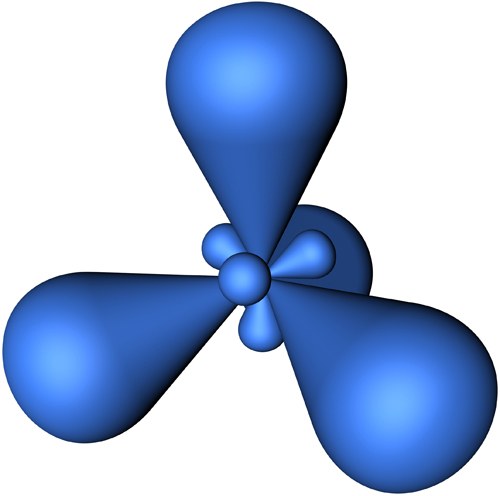
2. Атом углерода имеет sp3-гибридизацию орбиталей, которые располагаются под углом в 109 градусов и 28 минут. Перекрывание гибридных орбиталей происходит по прямой линии в горизонтальной плоскости.
3. Таким образом, при перекрывании орбиталей под таким углом образуется центрированный тетраэдр, тот, что относится к кубической системе, следственно дозволено сказать, что алмаз имеет кубическую конструкцию. Такая конструкция считается одной из самых крепких в природе. Все тетраэдры образуют трехмерную сеть из слоев шестичленных колец атомов. Такая устойчивая сеть ковалентных связей и трехмерное их разделение ведет к дополнительной прочности кристаллической решетки.
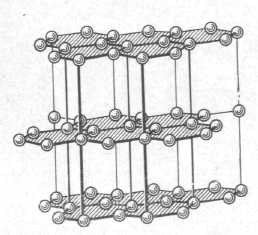
4. Кристаллическая решетка у алмаза довольно трудная. Она состоит из 2-х примитивных подрешеток. Область пространства, лежащая ближе к данному атому, чем к остальным атомам, для решетки алмаза представляет собой триакисов усеченный тетраэдр. Таким типом решетки владеют также кремний, германий и олово, предпочтительно альфа-форма.
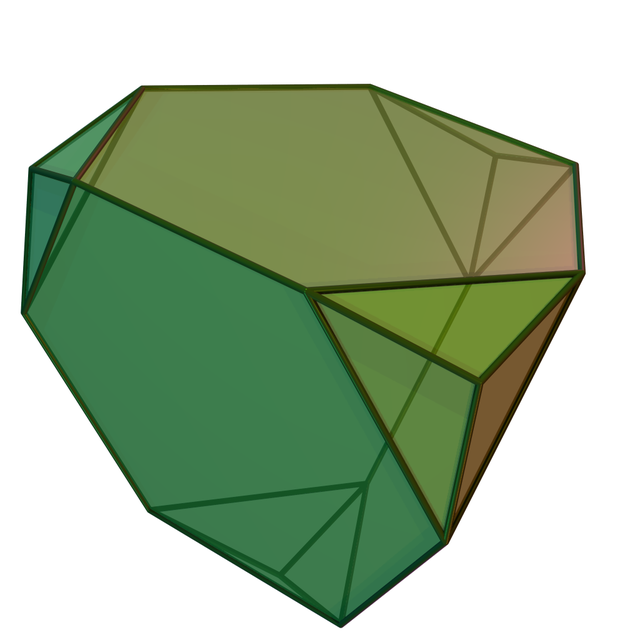
5. Триакисов усеченный тетраэдр представляет собой многогранник, сделанный из четырех шестиугольников и двенадцати равнобедренных треугольников. Он может быть использован для тесселяции трехмерного пространства. В качестве примера тесселяции дозволено разглядеть квадрат, тот, что нужно разрезать по диагонали, то есть тесселировать квадрат на два треугольника. Тесселяция сама по себе улучшает реализм трехмерной модели, а применительно к кристаллической решетке алмаза делает ее больше реалистичной.
6. На данный момент наука пришла к приобретению алмазов синтетическим методом. Для синтеза таких кристаллов применяют, как водится, высокоуглеродистый сплав никеля с марганцем либо высокочастотную плазму, сосредоточенную на подложке, где образуется сам алмаз. При приобретения минерала таким методом, его кристаллическая решетка крепко отличается от решетки, которую имеет настоящий алмаз. Происходит смещение слоев углерода, в связи с чем они располагаются хаотично. Именно следственно кристаллы, полученные таким методом, владеют меньшей прочностью и довольно высокой хрупкостью.









